defytime Science Japanの科学顧問であるビル・アンドリュース博士は、バイオテクノロジー産業の分野に30年以上もの間、身を置き、特にここ20年ほどは "ヒト細胞におけるテロメア短縮" へ介入することにより人間の寿命を延長する方法を探索することに焦点を当てています。
博士は、1981年にジョージア大学にて分子および集団遺伝学の分野で博士号を取得し、その後はArmos社およびCodon社にて上級研究員、Codon社およびジェロン(Geron)社にて分子生物学部門ディレクター、そしてEOS Biosciencesでは、技術開発部門のディレクターを歴任。
ネバダ州リノ市のバイオテクノロジー企業「Sierra Sciences, LLC」の創設者であり、現在、その社長および最高経営責任者を併任しています。
Sierra Sciences社では、ヒト細胞の内因性テロメラーゼの発現を一過性に誘導する薬物の発見に専ら取り組んでおり、既にそのような薬物を30種以上同定し、現在は、それらの作用機序の解明にも取り組んでいます。
ジェロン社での分子生物学部門ディレクター在任時に博士は、他の共同研究者らと共に"ヒトテロメラーゼ"のRNAおよびタンパク質両方の構成成分の発見に重要な貢献をし、1997年には本研究に対して米国の「その年の著名な国内発明家・発案者(National Inventor of the Year)」として第2位を受賞しました。
現在では、TAM-818などテロメラーゼに関する【50以上】もの米国発行の特許に発案者として、その名前を連ねています。
ビル・アンドリュース博士の世界での映像情報一覧はこちら >>>
ビル・アンドリュース博士の日本での講演会情報はこちら >>>
ビル・アンドリュース博士の著書等に関する情報はこちら >>>
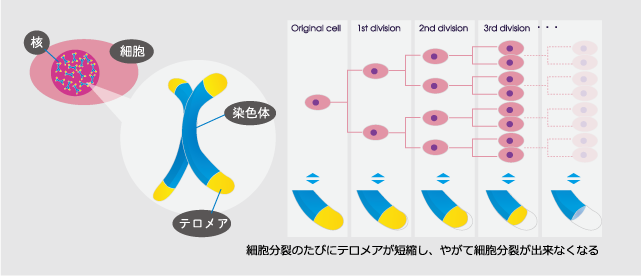
"テロメア(telomere)"は、ギリシャ語の「telos(末端)」と「meros(部分)」から作られた言葉です。繰り返し配列を持つDNAのかたまりで、染色体(直線状)の末端に存在しています。
このテロメアには、DNAの分解や修復から染色体を保護し、染色体の安定性を保つ働きがあります。
ご存知の通り人間は、数十兆の細胞から体を形成しており、これらの細胞が絶えず分裂活動をすることで、生命を維持しています。
しかし、染色体の正常な分配に必要とされるテロメアは、細胞が分裂する度に短縮してしまうため、テロメアが一定長より短くなると、染色体の不安定化がおこり細胞の生存性が失われ、結果として身体の様々な老化現象が現れます。
つまり、ヒトの老化の根本的な要因にテロメアが関係しているのです。
| 病名(英語) | 略語 | 病名(日本語) |
|---|---|---|
| CVD | 【心臓血管疾患】 | |
| - | 【癌】 | |
| COPD | 【慢性閉塞性肺疾患】 | |
| DDD | 【変性椎間板疾患】 | |
| AD | 【アルツハイマー病】 | |
| OA | 【変形性膝関節症】 | |
| RA | 【関節リウマチ】 | |
| - | 【骨粗鬆症】 | |
| - | 【全身免疫不全】 | |
| - | 【皮膚の老化】 | |
| AMD | 【加齢黄斑変性症】 | |
| - | 【肝硬変】 | |
| - | 【筋ジストロフィー】 | |
| - | 【細胞及び組織の移植】 | |
| AIDS | 【エイズ】 | |
| HGPS | 【プロジェリア症候群】 | |
| DC | 【先天性角化不全症】 | |
| IPF | 【特発性肺線維症】 | |
| - | 【ネコなき症候群】 | |
| DS | 【ダウン症】 | |
| FA | 【ファンコーニ貧血】 | |
| TS | 【結節性硬化症】 | |
| - | 【ウェルナー症候群】 | |
| - | 【老化】 |
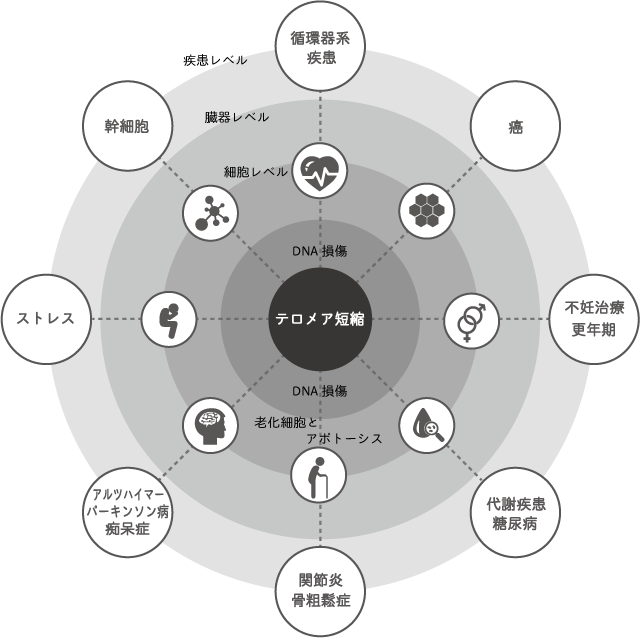
2009年ノーベル生理学・医学賞が3人の科学者に与えられ、世界的に大きな注目を集めているのが慢性疾患や早期診断を可能とする血液検査によるテロメア分析です。
この血液検査による「テロメア分析」では、前項にあげるような癌をはじめとする様々な病気への早期予後を可能とし、独立したバイオマーカーとしての役割は多大であり、今後の医療への貢献は非常に大きなものとなると世界中の医師からも注目されています。
その中でもdefytime Science Japanが進める分析は、ただ単純に平均的なテロメア長を推定するのではなく、全てのテロメアのヒストグラムを取り、短くなったテロメアを染色体ごとの割合も含め、総括的に評価する方法で、既に持つ膨大なデータによって加齢関連疾患のリスクを階層化するなど、適切に評価するアルゴリズムを有しています。

"2009年のノーベル医学生理学賞は、米カリフォルニア大のエリザベス・ブラックバーン(Elizabeth Blackburn)教授、ジョンズ・ホプキンズ大のキャロル・グレイダー(Carol W. Greider)教授、ハーバード大のジャック・ゾスタック(Jack W. Szostak)教授の3氏が受賞しています。受賞理由は、『寿命のカギを握るテロメアとテロメラーゼ酵素の仕組みの発見』でした。"テロメラーゼ"は、真核生物の染色体末端に存在するテロメアの特異的反復配列を伸長させる酵素です。しかし、ヒトにおいては、生殖細胞・幹細胞・ガン細胞などでの活性が認められており、それ以外のテロメラーゼ活性はほとんど見られません。
したがって、活性を高めることで「細胞分裂寿命の延長」、活性を抑制することにで「ガン治療」といった両面で注目を浴びています。
「TAM-818」は、2014年ビル・アンドリュース博士(シエラサイエンセズ社)が開発したテロメアの短縮を抑制する物質です。
1999年から研究を始め、6万近くの化学物質を調査して、ようやく2007年に第一の化学物質で薬剤のようなものを発見しました。
これが地球上ではじめて発見された薬剤で、皮膚の細胞実験でテロメラーゼの産出に成功しました。
(※この薬剤は、米国のT.A. SCIENCE社に特許及び製品権を譲渡し、「TA-65」として2007年に市場導入されています)
さらに検証を進め、40万近くの検証を経てC0314818を発見しました。メカニズムも科学的に証明しており、特許の取得もした物質です。それが【Telomerase Activation Molecule】テロメラーゼを誘導活性化する分子【TAM】なのです。 実際、この時発見された「TAM-818」と「TA-65」と比較テストでは、「TAM-818」のテロメア伸長効果をもたらすテロメラーゼ発現において「TA-65」の80~300倍強力であったという結果も出ています。
| Fortunately, the telomerase gene already exists in all our cells. That’s because the DNA in every one of our cells is identical: a skin cell, muscle cell, and liver cell all contain exactly the same genetic information. Thus, if the cells that create our sperm and egg cells contain the code for telomerase, every other cell must contain that code as well. |
|---|
>>>幸い、実際にはテロメラーゼ遺伝子を私達の細胞に挿入する必要はありません。なぜなら、テロメラーゼ遺伝子は、すでにそこにあるからです。DNAはどの細胞でも同一であり、皮膚細胞、筋細胞、肝細胞、そのどれもがまったく同じ遺伝情報を持っています。ですから、私達の精子や卵子を作り出す細胞がテロメラーゼのコードを持っているなら、他の細胞もみな、同じコードを持っているはずなのです。
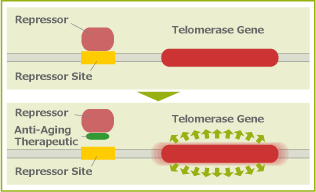
| The reason that most of our cells don’t express telomerase is that the gene is repressed in them. There are one or more regions of DNA neighboring the telomerase gene that serve as binding sites for a protein, and, if that protein is bound to them, telomerase will not be created by the cell. however, it is possible to coax that repressor protein off its binding site with the use of a small-molecule, drug-like compound that binds to the repressor and prevents it from attaching to the DNA. If we find the appropriate compound, we can turn telomerase on in every cell in the human body. |
|---|
>>>私達の細胞の大半がテロメラーゼを発現しないのは、その遺伝子が抑制されているからです。テロメラーゼ遺伝子に隣接するDNAには、特定のタンパク質との結合部位が一つもしくはそれ以上あり、タンパク質がそこに結合すると、細胞はテロメラーゼを作らなくなります。
しかし、リプレッサーと呼ばれるそのタンパク質に結合して、リプレッサーがDNAに結合するのを防ぐ低分子医薬品のような化合物を使えば、リプレッサー・タンパク質を結合部位から引き離すことができます。
適切な化合物を見つけることができれば、人体内のあらゆる細胞のテロメラーゼをオンにでき、細胞は何回でも必要な回数、正しく分裂できるようになります。